|
 I) INTRODUCTION
I) INTRODUCTION
A force d'utilisation, un percolateur se couvre d'un dépôt blanchâtre appelé tartre.
Pour détartrer un percolateur, on trouve dans le commerce des petits sachets de poudre sur létiquette desquels est inscrit « contient de lacide sulfamique ».
Le « de » nest guère précis. Nous allons déterminer le pourcentage dacide sulfamique présent dans cette poudre.
Suivant les fabricants le détartrant peut être à base d'acide sulfamique (plus fort, plus toxique), d'acide citrique (moins fort) ou encore d'un mélange des deux. Nous en avons même trouvé avec comme indication sur la boîte "à base d'acide sulfamique" et sur les sachets (dans la boîte) à "base d'acide citrique" (le consommateur est trompé et que dire au centre anti-poisons en cas d'intoxication ?
 II) AVANT DE COMMENCER ... quelques calculs préliminaires. II) AVANT DE COMMENCER ... quelques calculs préliminaires.
 Un dosage acide-base par volumétrie (titrage) nous semble tout indiqué pour ce travail. On suppose que la poudre ne contient quun seul acide, lacide sulfamique (certaines poudres peuvent contenir de lacide citrique moins efficace. Pourquoi ?). Nous allons donc utiliser une solution de NaOH comme titrant. Un dosage acide-base par volumétrie (titrage) nous semble tout indiqué pour ce travail. On suppose que la poudre ne contient quun seul acide, lacide sulfamique (certaines poudres peuvent contenir de lacide citrique moins efficace. Pourquoi ?). Nous allons donc utiliser une solution de NaOH comme titrant.
On va dissoudre exactement environ 1g de poudre dans un jaugé de 100mL. On titrera 20mL de cette solution.
Quelle devrait être la concentration du NaOH pour que le titrage soit réalisable ? Pour répondre à cette question, supposez que la poudre contient 100% dacide sulfamique.
 III) AU LABORATOIRE ... III) AU LABORATOIRE ...
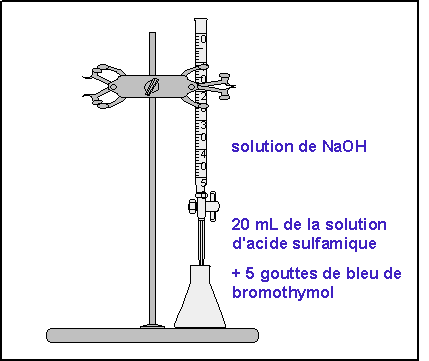 - Préparer 100 ou 250mL dune solution de NaOH dont la concentration a été calculée plus haut et validée par le professeur.
- Préparer une solution dacide sulfamique en dissolvant environ 1g (pesée précise !) de poudre dans 100mL deau (ballon jaugé).
- Remplir la burette avec la solution de NaOH.
- Mettre dans un erlenmeyer 20mL de la solution dacide sulfamique additionnée de 5 gouttes de bleu de bromothymol.
- Commencer par un titrage rapide (mL par mL) pour repérer approximativement le point équivalent.
- Recommencer (2 ou 3 fois) le titrage en veillant à déterminer avec précision (à la goutte près) le point équivalent.
On vous demande de déterminer le pourcentage dacide sulfamique dans la poudre.
 IV) POUR EN SAVOIR PLUS ... IV) POUR EN SAVOIR PLUS ...
 V) LES PRODUITS V) LES PRODUITS
Hydroxyde de sodium 0,1M
NaOH | M : 40,00
R36/38 irritant pour les yeux et la peau
|
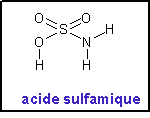
Acide sulfamique
H3NO3S | M : 97,09
R36/38 Irritant pour les yeux et la peau
R52/53 Nocif pour les organismes aquatiques
En cas de contact (yeux, peau) laver abondamment avec de l'eau.
|
|


 @t
home, ressources scientifiques (02/2006)
@t
home, ressources scientifiques (02/2006)

 @t
home, ressources scientifiques (02/2006)
@t
home, ressources scientifiques (02/2006)